
ĐẶT VẤN ĐỀ
Mục tiêu: bài báo này là một tóm tắt ngắn gọn các hiểu biết về sinh lý bệnh của rối loạn lo âu tính cho đến thời điểm hiện tại, cũng như các yếu tố nguy cơ góp phần đến sự xuất hiện và kéo dài của chúng, bài báo này cũng giúp nhìn lại về tiêu chuẩn chẩn đoán đi cùng tiếp cận điều trị đã được nhắc đến trong guideline Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5).
Mặc dù rối loạn lo âu xuất hiện mọi nơi trên toàn cầu, nhưng vẫn chưa có một thống nhất về mức độ chứng cứ của nó. Rối loạn lo âu có cơ chế rất phức tạp, là sự trộn lẫn giữa các yếu tố về sinh học con người, tâm thần học và môi trường tác động. Hiện nay, cơ chế của việc rối loạn chức năng não bộ là sinh lý bệnh được nhiều chuyên gia đồng thuận hơn cả. Điều trị rối loạn lo âu theo y học chứng cứ như các biện pháp tác động vào hành vi, cũng như sử dụng các thuốc chống trầm cảm được cho là có hiệu quả trên chu trình rối loạn chức năng não vừa nêu, thật ra đó là sự rối loạn của 1 chu trình khép kín, bao gồm sự kết nối có tính tương hỗ qua lại giữa vỏ não vùng trán trước lưng bên, thùy đảo và hạch hạnh nhân.
Tóm lại: Các rối loạn lo âu là các rối loạn về cảm xúc thường gặp nhất, và đang lan rộng ra mọi nơi
trên toàn cầu. Hiện nay, đã có nhiều cách điều trị hiệu quả khác nhau.
GIỚI THIỆU
Nỗi sợ là một cảm xúc có mặt trên tất cả các động vật có vú và nó cần thiết cho việc sống còn. Nỗi sợ được cho là kết quả của sự tác động qua lại của các yếu tố, cảm xúc, thái độ, hành vi khi cá thể đó gặp phải một tác nhân đe dọa đến từ môi trường, cho phép cá thể phản ứng lại bằng cách “tự vệ, tấn công hoặc bỏ chạy”. Ngược lại, lo âu là một cảm giác có xu thế hướng ở tương lai nhiều hơn, mà trong lo âu cá thể thường lo sợ một điều không được chắc chắn, và nó có thể không xẩy ra nếu không có đủ các điều kiện thúc đẩy. Mặc dù, nổi sợ và lo âu là 2 phạm trù khác nhau, nhưng nếu xét kỹ càng chúng có những điểm phân mảnh chung, mà điều này đã được chứng minh bằng các nghiên cứu trong lãnh vực thần kinh học. Lo âu có thể xuất hiện và giúp cá thể hướng đến một mối nguy có thể xuất hiện và qua đó giúp cá thể chuẩn bị về mọi mặt như sinh học, thái độ và tâm thần để sẵn sàng đáp ứng với mối nguy ấy. Nếu điều này kéo dài, không được kiểm soát, thì việc lo âu đó có thể trở thành bệnh ly thật sự.
Rối loạn lo âu là nhóm bệnh lý phổ biến nhất được nêu trong Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5). Rối loạn lo âu là các tình trạng mạn tính và không hề ổn định. Chúng được ước tính là xếp hàng thứ 6 trong việc gây ra giảm sức lao động trên toàn cầu, hơn cả đái tháo đường, COPD và thoái hóa khớp.
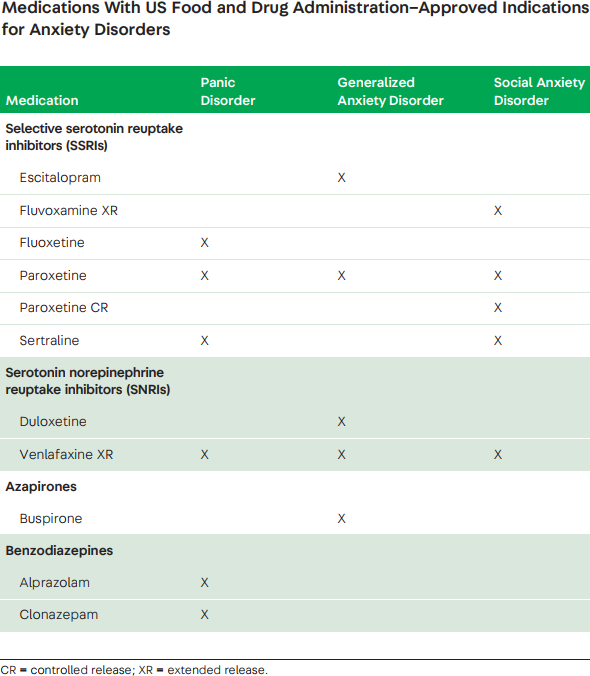

Các thuốc được FDA công nhận điều trị rối loạn lo âu
SINH LÝ BỆNH VÀ CÁC YẾU TỐ NGUY CƠ
Rối loạn lo âu là một hỗn hợp phức tạp của việc tương tác qua lại giữa các yếu tố: tâm thần, sinh học, và các yếu tố ngoại cảnh. Các nghiên cứu trên những cá thể có độ lo lắng cao đã tìm ra bằng chứng rằng việc khó khăn hay thiếu quyết đoán trong các tình huống quyết định là hệ quả cho việc tăng khuunh hướng dẫn đến các kết nối giữa các sự việc không hề liên quan nhau. Về mặt lâm sàng, đây là hệ quả của việc đánh gái quá cao yếu tố nguy cơ và đáp ứng kích thích thần kinh không phù hợp trước các mối nguy hiểm dẫn đến việc tăng hoạt hóa quá mức vòng lặp liên quan đến nổi sợ trong não cũng như các đáp ứng quá mức được quan sát thấy trên bệnh nhân rối loạn lo âu. Các bất thường về các chu
trình thần kinh não bộ cũng như các rối loạn chức năng đặc hiệu, có thể là cơ sở của việc rối loạn lo âu. Các kích thích độc hại là hoạt hóa một chu trình thần kinh trong não mà tôi tạm gọi là “chu trình đe dọa” “threat circuit”. Chu trình này được hình thành bằng sự kết nối của các thành tố như: vỏ anox trước trán vùng lưng bên, thùy đảo và hạch hạnh nhân.
Các nghiên cứu cho thấy, khi có các yếu tố đe dọa xuất hiện, chu trình này trên người bình thường sẽ được kích hoạt, và chu trình này bị tăng kích hoạt, đã được quan sát thấy trên các bệnh nhân có rối loạn lo âu. Fonzo và cộng sự đã báo cáo trong nghiên cứu của mình, các bệnh nhân mắc rối loạn lo âu chung, rối loạn lo âu xã hội và rối loạn hoảng sợ, ở từng thể có điểm khác nhau là sự kích hoạt trên
thể hạnh nhân cũng khác nhau, khi tiến hành thử nghiệm cho họ bài tỏ niềm hạnh
phúc cũng như nổi sợ trên khuôn mặt. Những người rối loạn kiểu hoảng sợ có sự tăng kích thích trên thủy đảo, mà điều này là độc nhất vô nhị. Dựa trên các nghiên cứu này mà rối loạn lo âu có thể phân loại dựa vào các đặc điểm tăng kích thích trên các vùng biệt định khi có mối đe doạn xuất hiện.
Nhiều yếu tố góp phần trong việc điều hòa “chu trình đe dọa” này. Chu trình này được chứng minh là sẽ bị ức chế bởi serotonin. Chính vì thế, bạn có thể thất, SSRIs chính là nhóm thuốc đầu tay để điều trị hàng loạt các rối loạn lo âu. Nó được chứng minh là làm giảm các kích thích điện não sinh học tại kết nối vỏ não vùng lưng bên – hạch hạnh nhân. Vỏ não trước trán vùng lưng bên được coi là có vai trò then chốt trong việc điều hòa cảm xúc, thông qua quá trình chú ý. Các điều trị chuyên về tâm thần cho rối loạn lo âu như liệu pháp chỉnh nhận thức – thái độ được cho là có tác dụng để thúc đẩy sinh học thông qua tăng cường kích hoạt hạch hạnh nhân. Giả thuyết đã đặt ra rằng, các điều trị theo chứng cứ có thể thúc đẩy việc giảm tiến trình theo kiểu từ dưới lên “bottom-up processing” (ví dụ như các thuốc chống trầm cảm) hoặc tăng cường kiểm soát từ trên xuống “top-down control” (như các liệu pháp thay đổi thái độ-hành vi). Thêm nữa, các yếu tố ngoại cảnh cũng được xác định là góp phần vào các rối loạn lo âu, cơ chế được cho là chúng kích hoạt quá mức sự kết nối giữa thùy trán trước vùng lưng bên và hạch hạnh nhân.
BIỂU HIỆN LÂM SÀNG
Bài báo này phân rối loạn lo âu theo DSM-5: rối loạn hoảng sợ, chứng sợ đám đông, rối loạn lo âu lan tỏa, hội chứng sợ giao tiếp xã hội, ám sợ chuyên biệt, chứng câm chọn lọc, rối loạn lo lắng bị xa cách, rối loạn lo âu do thuốc/các chất, và các rối loạn lo âu gây ra do các bệnh tình y khoa khác.
CƠN HOẢNG LOẠN VÀ RỐI LOẠN HOẢNG SỢ
Cơn hoảng loạn theo DSM-5 được định nghĩa là những con hoảng sợ rời rạc mà chạm đến tột cùng chỉ trong vài phút, trong cơn, các rối loạn dạng cơ
Đây được xem là một phân nhánh nhỏ trong rối loạn hoảng sợ, nhưng DSM-5 chia chứng sợ đám
thể và triệu chứng về nhận thức sẽ xuất hiện. Các cơn hoảng loạn không nhất thiết chỉ xẩy ra trên các bệnh nhân có rối loạn hoảng sợ, mà nó có thể xẩy ra trên các bệnh nhân có rối loạn tâm thần hoặc sinh lý khác. Theo dõi dấu hiệu sinh tồn là cách dễ dàng để chẩn đoán, ví dụ sự thay đổi dù là nhỏ trong hịp tim (vd tăng 7 nhịp/phút, chạm đến nhịp tim 90 l/p) là các dấu hiệu điển hình sẽ xảy ra trong cơn hoảng loạn. Cơn hoảng loạn có thể xảy ra bất kêt thời điểm nào, nhưng chủ yếu nó sẽ xuất hiện vào lúc nửa đêm kho các chức năng trong cơ thể bắt đầu giảm hoạt động. Để chẩn đoán cơn hoảng loạn thì bệnh nhân phải có cơn tái đi tái lại không đoán trước được và không phải do bệnh lý hoặc do thuốc uống, kéo dài ít nhất là 1 tháng.
Cơn hoảng loạn thường xuất hiện ở giai đoạn trễ của thời niên thiếu, 1/3 cuối giai đoạn cuộc đời. Các yếu tố nguy cơ là: giới nữ, tiền sử lo lắng lúc thời niên thiếu, ức chế hành vi, và tiền sử bị bạo hành.
Hầu hết các bệnh nhan có cơn rối loạn hoảng loạn đều có bệnh tâm thần đồng mắc, đặc biệt là rối loạn trầm cảm nặng, nhầm lẫn thuốc hoặc các rối loạn lo âu khác.
Cả điều trị tâm lý và bằng thuốc đều chứng minh có hiệu quả trên bệnh nhân có cơn rối loạn hoảng loạn. Điều trị rối loạn nhận thức – hành vi được xem là đầu tay cho rối loạn cơn hoảng loạn này. Điều thú vị, là các nghiên cứu đã chỉ ra việc kết hợp thêm thuốc so với các điều trị thay đổi thái độ – hành vi đơn độc không có sự khác biệt hay tăng hiệu quả gì thêm nếu sử dụng kết hợp thuốc. Các thuốc được FDA thông qua để điều trị rối loạn hoảng sợ bao gồm : SSRIs (eg, fluoxetine, paroxetine, and sertraline), serotonin norepinephrine reuptake inhibitors (SNRIs; eg, venlafaxine XR), và thuốc nhóm benzodiazepines (eg, alprazolam and clonazepam). Các dữ liệu điều trị cho thấy hiệu quả cải thiện triệu chứng đáng kinh ngạc (75%), song, đáng tiếc tỷ lệ hồi phục chức năng hoàn toàn vẫn còn thấp (12%) sau 3 năm điều trị.
CHỨNG SỢ ĐÁM ĐÔNG
đông khác với rối loạn hoảng sợ, được thấy rõ thông qua định nghĩa khác nhau. Chứng sợ đám đông
được đặc trưng bằng sự xuất hiện nổi sợ hoặc lo lắng về việc tiếp xúc với cộng đồng, kéo dài trên 6 tháng, với triệu chứng của sợ hoặc lo lắng xuất hiện hầu hết mọi thời điểm. Hậu quả là bệnh nhân tránh tiếp xúc với đám đông vì bệnh nhân lo lắng các triệu chứng sẽ xuất hiện hoặc sợ sẽ không thoát ra được các triệu chứng ấy. Những bệnh nhân mà đáp ứng cả 2 tiêu chuẩn sẽ được chẩn đoán vừa có rối loạn hoảng sợ và có hội chứng sợ đám đông kèm theo.
Theo thống kê, loại này gặp khoảng 2%. Hầu hết hay gặp ở người già, và thường có bệnh lý nội ngoại khoa kèm theo hoặc sau một biến cố nào đó, chẳng hạn như té ngã. Việc bác sỹ tách ra được chẩn đoán rối loạn hoảng sợ kèm hội chứng sợ đám đông hay chỉ hội chứng sợ đám đông đơn độc thôi là khá quan trọng cho việc điều trị, vì không có một bằng chứng nào cho đến hiện nay, rằng điều trị thuốc sẽ hiệu quả trên các bệnh nhân có hội chứng sợ đám đông nhưng không có rối loạn hoảng sợ kèm theo. Việc điều trị hiệu quả được lựa chọn nêu chỉ có hội chứng sợ đám đông riêng lẻ là cho bệnh nhân tiếp xúc dần với đám đông.
RỐI LOẠN LO ÂU LAN TỎA (GAD)
Là một dạng bệnh được đặc trung bằng việc lo âu hoặc lo lắng quá mức về nhiều vấn đề, và kéo dài trên 6 tháng, bệnh nhân khó tự kiểm soát và đi kèm với các triệu chứng thực thể. Về mặt lâm sàng, các bệnh nhân bị rối loạn lo âu lan tỏa thường lo lắng quá mức về các vấn đề nhỏ nhặt trong cuộc sống hoặc lo lắng về các sự việc không được chắc chắn, họ có khuynh hướng chú ý đến một cách vô thức đến các kích thích có tính đe doạn đến từ môi
trường sống. DSM-5 yêu cầu bệnh nhân phải có các triệu chứng tự động nhất quán quá mức hưng phấn (kích thích, căng cơ, mất ngủ, luôn cảng thẳng) và kiệt sức quá mức. Theo như khảo sát, chỉ 1/3 số người có triệu chứng rối loạn lo âu lan tỏa đi khám bệnh. Điều này có thể do nó không xuất hiện trong bối cảnh bị tâm thần. Cần lưu ý thêm, bệnh nhân có rối loạn lo âu lan tỏa thường xuất hiện các triệu chứng thực thể như: đau đầu, đau lưng, mất ngủ, viêm loét dạ dày, mà các vấn đề này họ thường đi khám nội khoa hơn là khám triệu chứng tâm thần.
Tần suất xuất hiên GAD trên toàn cầu trong một kiếp người vào khoảng 3-5%, thường sẽ xuất hiện và đạt đỉnh thời niên thiếu và giai đoạn sớm của
trưởng thành, đỉnh sau đó là sẽ vào giai đoạn 50-60 tuổi, có lẻ là do ở tuổi này nhiều bệnh mạn tính xuất hiện. Yếu tố nguy cơ cho mắc GAD gồm: nữ giới, nghịch cảnh thời thơ ấu và tình trạng kinh tế-xã hội thấp. Tỷ lệ cao các bệnh nội khoa và tình trạng tâm thần đồng mắc cũng được ghi nhận thấy trên các bệnh nhân GAD.
GAD là một tình trạng mạn tính và đòi hỏi điều trị lâu dài. Rất may, nó đáp ứng với cả điều trị tâm lý và điều trị thuốc, với tỷ lệ đáp ứng từ 30-50% trong cả 2 cách điều trị. Điều trị hành vi-nhận thức được cho là điều trị đầu tay. FDA đã thông qua các thuốc điều trị GAD gồm SSRIs (escitalopram and paroxetine), SNRIs (duloxetine and venlafaxine XR), và azapirones (buspirone). Hầu hết các chuyên gia công nhận benzodiazepines có vai trò điều trị bổ sung khi sử dụng ngắn hạn (3-6 tháng).Tuy nhiên, nhóm thuốc này nên tránh sử dụng trên các bệnh nhân hay lạm dụng thuốc. Thời gian khuyến cáo cho việc điều trị GAD là một năm (1 năm).
RỐI LOẠN LO ÂU XÃ HỘI (SAD)
Tần suất của loại rối loạn này chiếm đến 10% trên toàn cầu. Trong đó, phụ nữ chiếm đến 2/3 số lượng. Điển hình hay gặp ở lứa tuổi trung niên và sau đó thì khá không phổ biến gặp nữa. Chỉ một lượng nhỏ bệnh nhân có rối loạn lo âu xã hội tìm đến việc điều trị. Theo dữ liệu của Hoa kỳ, con số bệnh nhân có đủ triệu chứng và đến điều trị là dưới 10%. Đây là một tình trạng mạn tính và tỷ lệ hồi phục sau 5 năm với điều trị chiếm 25%.
Yếu tố lõi thường gặp trong rối loạn lo âu xã hội là sợ bị người khác đánh giá tiêu cực trong các hoạt động đoàn thể. Ví dụ, bệnh nhân có SAD, sẽ có nổi sợ quá mức hay không thực tế về các đánh giá cảu người khác trong các đoàn thể tham gia. Và đây là các tình huống sẽ là cho người có SAD vô cùng khó khăn: phát biểu và chú ý trước đám đông. Những người bị SAD có thể làm quá lên các khả năng các biến cố tiêu cực xuất hiện “chẳng hạn như không ai trong buổi tiệc thích tôi cả” dẫn đến chu trình đe dọa trong não kích hoạt các dấu hiệu thực thể như
nhịp tim cực nhanh, vã mồ hôi tay. Và khi rút ra khởi tình huống đám đông các dấu hiệu sẽ quay về
bình thường và rất không may nếu cứ tái diễn như thế sẽ dẫn đến tăng việc né tránh xã hội và lâu dần có thể dẫn đến các rối loạn nguy hiểm hơn như trầm cảm và làm bệnh nhân né tránh xã hội hơn nữa. Các nghiên cứu ngẫu nhiên có đối chứng dã chỉ ra điều trị bằng thay đổi thái độ-hành vi cũng như thuốc sẽ có hiệu quả cho loại rối loạn này. FDA đã thông qua các thuốc dùng để điều trị SAD bao gồm: SSRIs fluvoxamine XR, paroxetine, paroxetine CR, và sertraline và nhóm thuốc SNRI venlafaxine XR.
Nếu nổi sợ hoặc lo âu được hạn chế ở việc sợ phát biểu hoặc sợ thể hiện trước cộng đồng, thì nhóm thuốc beta-blocker được xem là thuốc với chỉ định phụ cho việc sợ thể hiện trước đám đông.
ÁM ẢNH CỤ THỂ
Loại rối loạn này ước tính chiếm tới 7.4%. Ám ảnh môi trường tự nhiên (vd sợ nước hay độ cao) là loại phổ biến nhất, sau đó sẽ là sợ các tình huống (như bay), sợ động vật, sợ vết thương – chảy máu (sợ kim tiêm). Ngược lại với các loại rối loạn khác, sợ vết
thương – chảy máu sẽ làm giảm hơn là là làm tăng các hoạt động hệ thần kinh giao cảm, dẫn đến bệnh nhân có thể ngất hoặc phản xạ vagal. Thường loại sợ này sẽ xuất hiện vào thời điểm thập kỷ đầu của cuộc đười mổi người. 2/3 thường xuất hiện ở phụ nữ. Điều trị chủ yếu là thay đổi thái độ hành vị và cho thử tiếp xúc. Không có một loại thuốc nào được FDA thông qua đẻ điều trị loại ám ảnh này, mặc sử dụng nhóm thuốc benzodiazepine ngắn hạn cho các bệnh nhân khi không thể tránh khỏi phải đối mặt (như đi máy bay) hoặc các thuốc chẹn beta như propranolol thì không phổ biến sử dụng.
ĐIỀU TRỊ CÁC RỐI LOẠN LO ÂU
Hiện nay, có nhiều cách hiệu quả để điều trị rối loạn lo âu, bao gồm cả can thiệp tâm thần lẫn sinh học.
Phần tiếp sau đây sẽ đưa ra các tiếp cận điều trị rối loạn lo âu.
TIẾP CẬN CHUNG ĐỂ ĐÁNH GIÁ LO ÂU
Bước quan trọng nhất trong điều trị lo âu là tim cho ra nguyên nhân, yếu tố thúc đẩy, và khoảng thời
gian mà bệnh nhân đã phải chịu đựng triệu chứng. Để đạt được các điều này, cần phải hỏi ra bản chất của triệu chứng (ví dụ như lo lắng, triệu chứng dạng cơ thể hay thái độ tránh né), các yếu tố mồi cho cơn lo âu (ví dụ như các biến cố trong cuộc sống, bệnh nội khoa, thay đổi thuốc, lạm dụng thuốc), cũng như những suy ngẫm và niềm tim của bệnh nhân về chính nổi lo âu của mình. Ví dụ lo âu và tránh né các tiếp xúc xã hội có thể đến từ việc tụt cảm xúc và giảm các niềm vui thích (rối loạn trầm cảm), hoặc liên quan đến nổi sợ bị người khác đánh giá mình (rối loạn lo âu xã hội), hoặc bị chia cắt với người yêu (rối loạn lo lắng xa cách), hoặc sợ sắp đi máy bay…Các rối loạn lo âu ngắn hạn này có thể được điều trị triệu chứng bằng việc hỗ trợ, tái đánh giá và nếu cần có thể điều trị ngắn hạn bằng nhóm benzodiazepine.
Rối loạn lo âu là một chẩn đoán đi kèm với việc phải loại trừ các bệnh lý góp phần cho rối loạn lo âu xẩy ra. Vì vậy nên khám nội kỹ càng để loại các bệnh nội ngoại khoa có thể ẩn bên dưới. Các yếu tố có thể gợi ý khả năng rối loạn lo âu này là do một bệnh lý nội khoa tiềm ẩn như: chưa có tiền căn rối loạn lo âu trước đó, khởi phát lo âu giai đoạn trễ hơn bản chất của loại rối loạn đó, có sự thay đổi gần đây của việc điều trị bệnh nội khoa nền hoặc thay đổi toa thuốc, và sự xuất hiện các triệu chứng không điển hình như mất tri giác, mất kiểm soát bàng quang, hoặc ngất trong suốt cơn hoảng loạn. các guidelines khuyến cáo nếu nghi ngờ bệnh tiềm tàng thì các xét nghiệm sau nên được chỉ định: công thức máu, điện giải, đường huyết đói, (TSH), độc chất nước tiểu và ECG.
Các guidelines lâm sàng chỉ ra các rối loạn lo âu có thời gian ngắn hạn đáp ứng với điều trị từ 50-60%. Việc tiếp cận và điều trị theo từng bước dựa trên độ nặng của bệnh nhân là cần thiết. Và độ nặng của rối loạn lo âu có thể được đánh giá thông qua bảng câu hỏi. Nhiều nghiên cứu đã xác nhận giá trị của thang điểm Generalized Anxiety Disorder 7-Item Scale (GAD-7) trong việc tự đánh giá rối loạn lo âu. Đay là một bảng câu hỏi mà
trong đó cso 7 câu hỏi với tổng điếm từ 0-21. Và ở mổi mức sẽ xếp độ nặng theo từng thang điểm, với mức độ nhẹ thì chỉ cần tiếp cận tâm lý và trông chừng họ. Nếu từ mức độ trung bình trở lên thì điều trị thay đổi thái độ và có thể dùng thuốc kèm theo nên được sử dụng. Còn với mức độ nặng hoặc lo âu kháng trị thì chắc chắn nên kết hợp thêm thuốc bên cạnh điều trị thay đổi nhận thực-hành vi.
TIẾP CẬN ĐIỀU TRỊ VỚI TRIỆU CHỨNG MỨC ĐỘ NHẸ
Bệnh nhân và người thân nên được định hướng lại bản chất của rối loạn lo âu, bao gồm triệu chứng cả mặt tâm lý học và sinh lý học, các điều trị có sẵn để lựa chọn. Các chuyên gia lâm sàng nhận thấy sẽ có lợi ích nhất nếu bác sỹ cùng thảo luận và nhấn mạnh tính phổ biến của rối loạn lo âu, các nguyên nhân di truyền và tỷ lệ hồi phục ngoạn mục sau điều trị.
Bệnh nhân cũng nên được nhắc tránh các yếu tố thúc đẩy việc lo âu như café, bia rượu và các thuốc kích thích. Các chất có tính an thần như bia rượu có thể làm dịu cơn lo âu nhưng nó sẽ làm bùng lên cơn hoảng loạn , lo âu trong giai đoạn withdrawal (rút lui). Bệnh nhân nên được khích lệ để tập thể thao và làm các bài tập thư giản.
TIẾP CẬN ĐIỀU TRỊ VỚI TRIỆU CHỨNG TRUNG BÌNH
Với mức độ này tiếp cận sẽ là điều trị thay đổi thái đội hành vi hoặc thuốc hoặc sử dụng cả hai. Các dữ liệu về hình ảnh học thần kinh cho thấy hiệu quả của 2 mô thức điều trị này là như nhau. Trong một nghiên cứu có thời gian dài, khảo sát nhóm bệnh nhân vừa được điều trị bằng các liệu pháp thay đổi thái độ hành vi đồng thời sử dụng nhóm thuốc SSRIs, nghiên cứu chỉ ra chẳng có sự khác biệt gì khi chỉ sử dụng liệu pháp thay đổi thái độ hành vi đơn lẻ, mặc dù việc kết hợp thêm thuốc được cho là sẽ có hiệu quả trong các trường hợp lo âu nặng hoặc lo âu kháng trị. Trước khi điều trị, bệnh nhân nên được biết rằng các triệu chứng lo âu có thể nặng lên giai đoạn đầu khi dùng thuốc hoặc khi bệnh nhân phải đối mặt với nổi sợ.
LIỆU PHÁP TÂM LÝ
Điều trị thay đổi hành vi nhận thức là một dạng điều trị tâm lý mà mục tiêu là hướng đến thay đổi suy nghĩ và thái độ đã là căn nguyên dẫn đến nổi lo của bệnh nhân. Mục tiêu của điều trị này là nhận diện và thách thức các nhận thức sai đồng thời hạn chế tối thiểu việc tránh né. Điều này có được bằng các buổi điều trị giữa nhà trị liệu và bệnh nhân để tập trung giải quyết vấn đề. Hiệu quả cảu phương pháp này đã được minh chứng rõ ràng và nó được chỉ định như điều trị đầu tay trong rối loạn lo âu. Một nghiên cứu rất lớn được thực hiện năm 2016 đã cho thấy hiệu quả không thể bàn cãi của phương pháp này, với number needed to treat cho từng loại lo âu là:1.42 cho rối loạn hoảng sở , 2.54 cho rối loạn lo âu lan tỏa và 2.54 cho rối loạn lo âu xã hội.
Tiếp xúc với nỗi sợ giúp bệnh nhân tăng khả năng đối diện nhưng đồng thời vùng an toàn giúp bệnh nhân tiệt trừ nỗi sợ thông qua việc học tập và rút kinh nghiệm bản thân. Những cách khác được sử dụng trong thay đổi thái độ hành vi là áp dụng bài tập thư giản cũng như kỹ thuật thở để giảm triệu chứng. Điều trị tâm lý là nền tảng cơ bản cho các rối loạn lo âu như: sợ những điều cụ thể, sợ đám đông, sợ phân ly, câm có chọn lọc.
Mặc dù bằng chứng đã chỉ ra điều trị thay đổi thái độ hành vi đạt hiệu quả cao, nhưng thống kê cho thấy phần lớn bệnh nhân không nhận được loại điều trị này, mặc dù họ thích nó hơn là sử dụng thuốc.
Rào cản cho việc này bao gồm: số lượng hạn chế của các chuyên gia đã được tập huấn về phương pháp điều trị thay đổi thái độ hành vi, nó tốn thời gian và nhiều tiền bạc, nổi sợ bộc lộ bản thân mình với chính nhà điều trị. Các nghiên cứu chỉ ra, việc điều trị tâm lý qua internet cũng có hiệu quả tương tự như kiểu trực tiếp face to face. Việc thiền định cũng được nghiên cứu và chỉ ra là giảm lo âu thông qua cơ chế kích hoạt vùng vỏ vành đai trước, vỏ não trán trước và thùy đảo trước.
Các thuốc phổ biến được sử dụng điều trị rối loạn lo âu
THUỐC
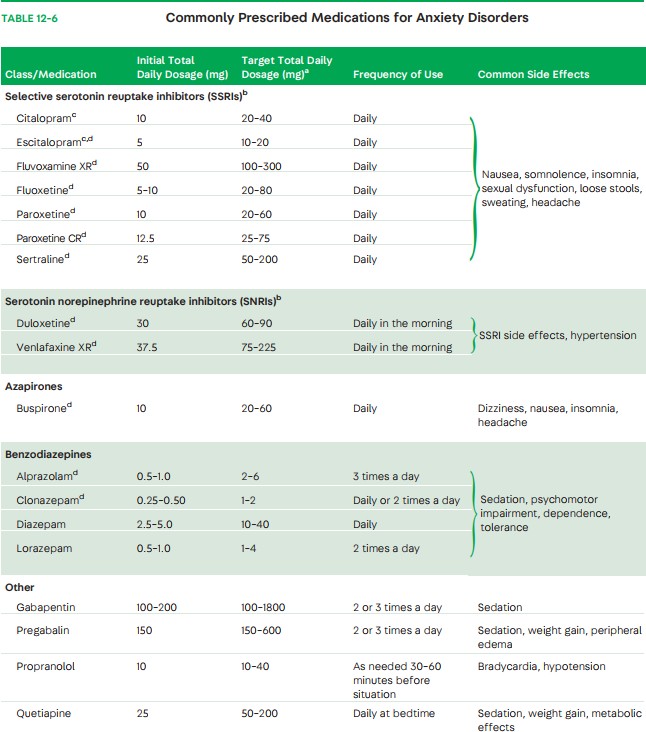

4 nhóm thuốc được FDA công nhận là có hiệu quả để điều trị rối loạn lo âu là: SSRIs, SNRIs, azapirones, và nhóm benzodiazepines. Nhiều nghiên cứu và các hướng dẫn lâm sàng đề nghị SSRIs và SNRIs là 2 nhóm thuốc điều trị đầu tay cho rối loạn lo âu. Các thuốc sẽ được tóm tắt trong các bảng bên dưới. Quan trọng nên nhớ là các nhóm thuốc này không chỉ có mổi chỉ định cho việc điều trị rối loạn lo âu, khuyến cáo nên sử dụng liều thấp lúc đầu và tăng dần liều với mổi bước nhảy từ 2-4 tuần, nếu bệnh nhân đã dung nạp, để đạt được ngưỡng điều trị (range).
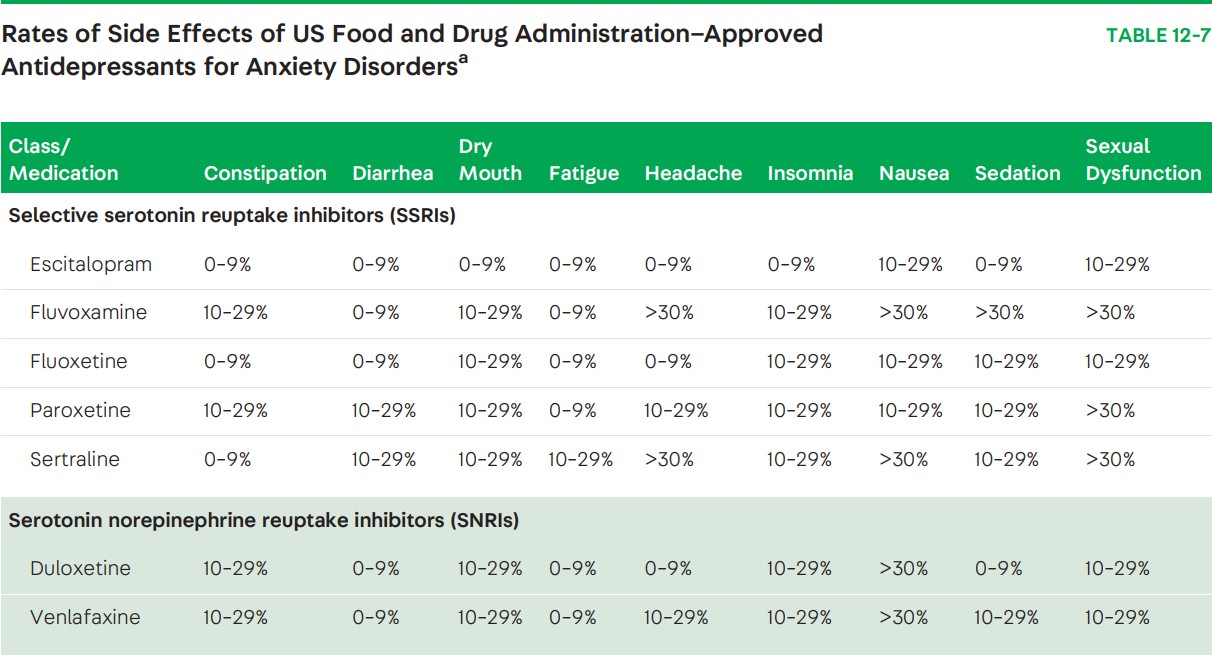

Tỷ lệ xuất hiện tác dụng phụ theo FDA ghi nhận
CÁCH CHỌN THUỐC
Trong khi không có một xét nghiệm nào nhằm giúp đánh giá hiệu quả điều trị, thì cuối cùng vẫn chỉ dựa vào các yếu tố lâm sàng mà thôi. Đầu tiên là chẩn đoán chuyên biệt. Như đã lưu ý trước đó, nhiều rối loạn lo âu đáp ứng tốt với thuốc chống trầm cảm.
Ngược lại, buspirone lại bị giới hạn điều trị kém với lo lâu lan tỏa. Buspirone, một thuốc nhóm azapironem không hiệu quả trên GABA. Tương tự các thuốc chống trầm cảm khác, buspirone cần 2-4 tuần để tác dụng hiệu quả, vì thế nó không hợp cho lo âu cấp tính. Còn nhóm beta-bloker như propranolol lại hiệu quả chỉ trên các bệnh nhân có rối loạn thể hiện trước đám đông. Propranolol liều 20-40mg sẽ hiệu quả nếu bệnh nhân uống trước 30 phút khi ra đám đông chẳng hạn như chuẩn bị thuyết trình. Thuốc này có thể hạn chế tối đa các biểu hiện ngoại biên của lo âu chẳng hạn như run.
Nên nhớ các bệnh tắc nghẽn hoặc hạn chế đường thở là chống chỉ định của nhóm thuốc này.
Việc đánh giá các triệu chứng trầm cảm kèm theo cũng giúp định hướng sử dụng thuốc, triệu chứngtraafm cảm thường sẽ đi kèm với rối loạn lo âu, mà nhóm benzodiazepine sẽ kém hiệu quả trị
trầm cảm, lúc này khuyến cáo nên sử dụng SSRIs hay SNRIs. Do tỷ lệ đáp ứng giữa các thuốc gần như nhau nên chọn thuốc nào thì còn lại dựa vào bản chất tác dụng phụ của thuốc ấy, cũng như hiểu biết rõ ràng của bác sĩ về thuốc đó. Các tác dụng phụ phổ biến nhất cảu nhóm thuốc SSRIs đó là: khó chịu dạ dày, an thần, mất ngủ và rối loạn hoạt động tình dục. Các tác dụng phụ như rối loạn cương
dương sẽ gặp ở vài người chứ không phải tất cả mọi người. Paroxetin là thuốc có hoạt tính kháng cholinergic cao hơn hẳng các thuốc khác thuộc nhóm SSRIs. Việc kháng cholinergic này có thể dẫn đến suy giảm nhận thức, đặc biệt trên người già và các bệnh nhân có bệnh lý não trước đó. Các thuốc chống trầm cảm 3 vòng cũng có hiệu quả điểu trị lo âu nhưng nó không được khuyến cáo sử dụng dù là second choice (điều trị thứ cấp), bởi vì nó gây tụt HA tư thế, độc tim mạch và gây kháng cholinergic.
Khi chọn thuốc, một điều quan trọng nữa là đánh giá khả năng tự sát của bệnh nhân. Theo một nghiên cứu các bệnh nhân có rối loạn ám ảnh cưỡng chế là những người có nguy cơ nghĩ đến tự sát cao hơn cả. Trên các bệnh nhân rối loạn lo âu kèm tụt cảm xúc là nhóm bệnh nhân nguy cơ tự sát cao hon khi sơ với chỉ có rối loạn lo âu hoặc chỉ có tụt cảm xúc
đơn lẻ. Trên các bệnh nhân này, cần chọn thuốc không làm tăng nguy cơ tự sát cũng như nguy cơ uống quá liều gây tử vong.
Một điều quan trọng nữa là đánh giá tình trạng sử dụng bia rượu của bệnh nhân. Thuốc nhóm benzodiazepine nên tránh sử dụng cho các bệnh nhân có tiền căn lạm dụng các chất kích thích. Hiện nay, tại Mỹ nhóm thuốc này đang sử dụng với tỷ lệ ngày càng cao ở người già, nhưng dù vậy việc sử dụng nó nên được tránh ở nhóm người già vì nguy cơ té ngã, an thần quá độ và làm suy nhận thức.
TIẾP CẬN ĐIỀU TRỊ RỐI LOẠN LO ÂU NẶNG VÀ CÁC THỂ KHÔNG ĐÁP ỨNG VỚI ĐIỀU TRỊ
Rối loạn lo âu là một tình trạng mạn tính và có các vòng lặp theo thời gian. Có rất nhiều yếu tố tác động đến việc kháng trị. Các nghiên cứu chỉ ra rằng yếu tố chiếm tỷ lệ cao nhất đó là bệnh nhân bỏ trị giữa liệu trình, sau khi đánh giá chẩn đoán đã chính xác chưa thì bước tiếp theo là đánh giá liệu đã cho
đủ liều và đủ thời gian điều trị chưa. Các nghiên cứu chỉ ra các thuốc chống trầm cảm nên điều trị với thời gian tối thiểu là 8-10 tuần, trong đó 2 tuần hoặc hơn nên sử dụng liều dung nạp cao nhất có thể. Nếu hiệu quả, thuốc chống trầm cảm nên được duy trì ở liều dung nạp cao nhất trong 9-12 tháng nhằm tránh tác động vòng lặp. Còn với liệu trinhg tâm lý thì điển hình nên là 12-16 buổi.
Với các bệnh nhân thất bại với thuốc SSRI thì một thuốc khác cũng thuộc nhóm SSRI nên được thử dùng. Nếu đến cỡ đó rồi mà bệnh nhân vẫn không đáp ứng thì khuyến cáo chuyển sang nhóm SNRI như duloxetine hoặc venlafaxine
Pregabalin, một thuốc dùng để điều trị động kinh, đau kiểu thần kinh, đau cơ xơ hóa, có hiệu quả trong điều trị rối loạn lo âu lan tỏa. Nó là một GABa không gắn với thụ thể benzodiazepine, khi kết hợp với buspirone không gắn benzzodiazepine, nó tỏ ra hiệu quả trên các bệnh nhân có tiền căn lạm dụng bia rượu.
Thank you


 Thank you
Thank you